Cellen in winterslaap
Wanneer cellen onherstelbaar beschadigd raken, kan dat tot diverse ouderdomsziekten leiden. Denk aan dementie, orgaanfalen maar ook aan kanker. Moleculair bioloog Peter de Keizer van het UMC Utrecht heeft een manier gevonden om die zogeheten ‘senescente' cellen op te ruimen. Dit is een zeer hoopvolle stap om in de toekomst kanker en andere aandoeningen te voorkomen en te genezen.
Ons hele leven door raken de cellen in ons lichaam beschadigd. Die DNA-schade kan ontstaan door ‘normale’ veroudering, maar ook door bijvoorbeeld externe factoren, zoals te veel zonlicht, ons dieet of roken. Ons lichaam herstelt de meeste schade, maar soms blijft er een beetje achter. Op een gegeven moment is er te veel dat niet meer kan worden gerepareerd. Cellen kunnen dan ‘senescent’ worden (van het Latijnse woord voor verouderen).
Die senescente cellen zijn dus onherstelbaar beschadigd, maar gaan niet dood. Zo vormen ze bij wijze van spreken een soort roest in onze organen. Zelf functioneren ze vaak nog best goed. Het probleem is echter dat ze chronisch allerlei stoffen hun omgeving in sturen. En die zorgen weer voor mini-ontstekingen en verstoren de communicatie met en in buurcellen. Zie het als een soort zand dat in een motor komt.
Op die manier versnellen senescente cellen veroudering, en dragen ze bij aan het agressiever worden van allerlei ziekten. Resultaten bij proefdieren hebben laten zien dat die onherstelbaar beschadigde cellen bijdragen aan onder meer kanker, het verlies aan spiermassa en -kracht, leverschade, hart- en vaatziekten en vormen van neurodegeneratie (ziekten aan het zenuwstelsel).
Peter de Keizer is associate professor in het UMC Utrecht. Hij heeft zijn levenswerk gemaakt van senescente cellen. Na meer dan 15 jaar onderzoek en testen in het lab, bij onder meer proefdieren, is het nu bijna tijd om te kijken of zijn bevindingen ook werken bij mensen. In het UMC Utrecht gaan namelijk klinische studies bij mensen met kanker starten, aan de hand van Peters onderzoek. Een interview met een volhardend onderzoeker...
Wat trok je zo aan in die senescente cellen?
“Ik ben extreem gefascineerd door de moleculaire biologie van ouder worden: wat maakt precies dat we verouderen? We kunnen aan de buitenkant zien dat we verouderen, maar wat gebeurt er op het kleinste niveau bij ons van binnen, in onze cellen en moleculen? Gewoon door te leven, raken cellen in ons lichaam continu beschadigd, verliezen ze hun functie, en kunnen ze uiteindelijk kanker en allerlei verouderingsziekten veroorzaken.”
“Ik ben altijd ontzettend nieuwsgierig geweest naar hoe dit proces werkt en hoe we het kunnen stoppen. Hoe kan het dat de ene cel wel in winterslaap gaat, en de andere niet? En hoe kan ik als moleculair bioloog vernieuwende manieren en uiteindelijk geneesmiddelen vinden om die senescente cellen te vernietigen?”
Wat hebben senescentie en kanker met elkaar te maken?
“Senescentie is een stressreactie in cellen nadat ze heftig of onherstelbaar worden beschadigd. Dit kan gebeuren in normale cellen, maar ook in kankercellen. En senescente cellen kunnen ook op een andere manier aan de ontwikkeling van kanker bijdragen. Zo scheiden ze ontstekingsbevorderende eiwitten uit, waardoor kanker wordt gestimuleerd en uitzaaiingen kunnen ontstaan. Verder kunnen senescente cellen zelf uitgroeien tot kanker als hun DNA op een bepaalde manier gaat muteren.”
Zijn alle senescente cellen hetzelfde?
“Nee, er zijn ontzettend veel types, en dat maakt ze juist zo lastig te bestrijden. Van één soort weten we inmiddels dat daar specifieke scars (littekens) in het DNA zijn ontstaan. We spreken dan van scarred senescence of scarred cancer. Er is sprake van een onherstelbare beschadiging. Dit type begrijpen we nu veel beter, en we geloven dat het een grote impact kan hebben als we juist die cellen vernietigen.”
“We komen die zware littekens in het DNA bijvoorbeeld tegen bij een kwart tot een derde van patiënten met uitgezaaide darm-, eierstok- of borstkanker. En juist om dat type kankercellen te vernietigen, hebben we een speciale zogeheten ‘CPP’ (celpenetrerende peptide – red.) ontwikkeld in het lab.”
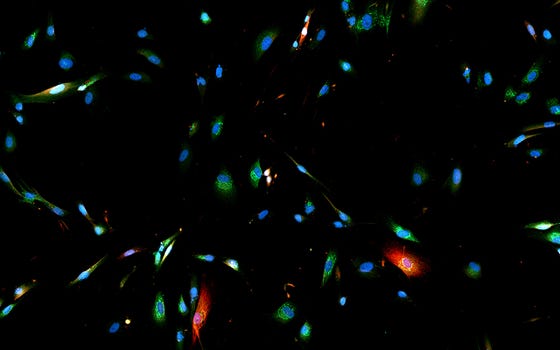
Een groep senescente RPE1 cellen (blauw), waarin grote verschillen bestaan in wat ze uitscheiden (rood en groen). Hiervoor is het belangrijk om stoffen te maken die specifiek de meest verkeerde senescente cellen aanpakken. Dit doen wij door bijvoorbeeld specifiek tegen PMLhoge littekencellen peptiden te ontwikkelen. Legenda: DNA (blauw), MMP3 (rood), IL1-β (groen) Data van Dr. Peter de Keizer and Dr. Johannes Lehmann
Een CPP, wat is dat precies?
“Dat is een molecuul dat door het membraan van cellen heen kan en zo stofjes naar binnen brengt om daar hun werk te doen. In dit geval is hun missie: ruim de littekencellen op. Hoe ze dat doen? In littekencellen is het eiwit p53 op verschillende plekken negatief geladen. Dat betekent dat de omgeving van het eiwit daar een minder hoge zuurgraad, oftewel pH-waarde, heeft. Littekencellen blijven in leven doordat het negatief geladen p53-eiwit chemisch verbonden is aan een ander eiwit: FOXO4. We hebben een CPP gemaakt die de twee eiwitten van elkaar losmaakt. Daardoor gaan de littekencellen dood.”
Hebben jullie het middel al getest?
“Bij muizen bleek onze aanpak succesvol: de gezondheid van muizen, die snel verouderen, werd verlengd. Na verder onderzoek, hebben we nu een CPP-versie die nog specifieker werkt tegen littekencellen: bij muizen van 800 dagen oud werd de gezonde levensduur van de muizen met 27 procent verlengd.”
Kan ik meedoen aan Peters klinische onderzoek?
De klinische onderzoeken staan nog niet gepland. De onderzoekers hopen begin 2027 toestemming te krijgen, afhankelijk van onder meer financiering. Op dit moment kunnen mensen zich dan ook nog niet aanmelden. Meer informatie volgt zodra dat mogelijk is.
Is er ook getest tegen kanker?
“Ja, we zagen al bij muizen met kanker dat het aantal uitzaaiingen van darm- en borstkanker naar de lever verminderde. Dit werkt ook vooral goed wanneer het eiwit p53 gemuteerd is, wat een groot probleem is bij de bestrijding van vele soorten kanker.”
“Daarnaast zagen we dat de CPP voorkwam dat borstkankercellen zich verder door het lichaam van de muizen verspreidden. Dit wordt allemaal nog grondig verder bestudeerd, inclusief doseringsschema's, doseringsfrequenties en te gebruiken oplosmiddelen. Uiteindelijk willen we dit goed en grondig testen in klinische studies, maar het ziet het er in elk geval al opwindend uit.”
Wanneer gaan jullie het middel proberen bij mensen?
“Studies naar de veiligheid bij dieren zijn inmiddels afgerond. Nu zijn we aan het kijken welke behandelschema’s het beste zouden kunnen werken. Afhankelijk van voldoende financiering en verder bewijs van werkzaamheid bij muizen, starten de klinische studies met mensen naar verwachting in 2027. Het gaat dan om patiënten met mutant-p53-borst- en darmkanker.”
Waarom specifiek bij die kankertypes?
“Juist bij deze soorten kanker vindt bijzonder veel scarring plaats, vooral wanneer ze verder gevorderd zijn. We hadden ook andere types kanker kunnen uitkiezen, maar juist vanwege de hoge mate van scarring bij borst- en darmkanker, hopen we sneller positieve resultaten te boeken tijdens onze eerste klinische trials.”
Waarom is er meer scarring bij deze kankersoorten?
“Het eiwit p53 is vaak gemuteerd bij deze types kanker en neemt daarom een andere vorm aan. Voor zulke gemuteerde p53-varianten werkt onze CPP ook en misschien zelfs beter. Dat is spannend, omdat deze kankers over het algemeen moeilijker te behandelen zijn met immuuntherapie en conventionele chemo- en radiotherapie.
“Ons onderzoek biedt dus hopelijk nieuwe behandelingsmogelijkheden voor kanker met gemuteerde vormen van p53. Als de eerste resultaten van de klinische trials positief zijn, zullen we ook kijken of het bij andere kankersoorten werkt.”
De klinische trials gaan over het genezen/terugdringen van kanker. Maar kan (de uitzaaiing van) kanker ook worden voorkomen door senescente of littekencellen op te ruimen?
“Dat willen we heel graag. Senescente cellen scheiden stoffen af die hun omgeving beschadigen. Omliggende cellen worden dus aangetast, en daardoor verergert de kanker. Door de meest problematische senescente cellen te vernietigen, de littekencellen denken we, kunnen we er wellicht voor zorgen dat de kanker minder snel verslechtert of uitzaait.”
“Uitzaaiingen zijn vaak moeilijk te bestrijden, maar we hebben ze al flink zien verminderen tijdens muisstudies. Dit is een belangrijke ontwikkeling, omdat we vaak zien dat de hoofdtumor wel goed behandeld kan worden, maar de uitzaaiingen die eruit ontstaan niet. We hopen tijdens de klinische studies ook bij mensen te zien dat de kanker minder vaak terugkeert of uitzaait.”
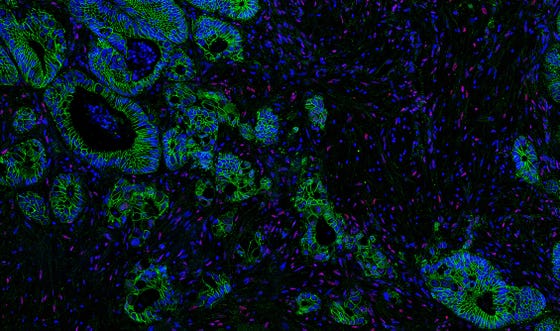
Uitzaaiing van een darmtumor (groen) naar de lever. Op sommige plaatsen zitten naast de tumor PMLhoge senescente cellen, die we littekencellen noemen. Wij bestuderen o.a. hoe signalen van deze littekencellen de kankercellen agressiever kunnen maken. Legenda: DNA (blauw), PML (rood), β-Catenine (groen). Data van Dr. Peter de Keizer en Dr. Johannes Lehmann
Wat zijn, naast de klinische studies, andere 'senescente vragen' waar je nu aan werkt?
“We proberen ook andere typen senescente cellen in kaart te brengen. Zo willen we erachter komen bij welke ziekte welk subtype van senescentie actief is. Ook willen we onderzoeken waarom omliggende cellen verstoord raken door senescente cellen. Wat gebeurt er precies met deze cellen, en wat betekent dat voor het ontstaan van kanker en andere verouderingsziekten?”
“Senescente cellen spelen een brede rol bij veroudering in het algemeen. Daarom zullen we bij onze klinische studies met kankerpatiënten ook verschillende factoren onderzoeken die veroudering meten. Hier in het UMC Utrecht werken we in een enorme hub van kennis, data en nieuwe technieken. En artsen zijn altijd dichtbij en bereid om met ons mee te denken. Inmiddels werken we binnen het UMC Utrecht ook samen aan projecten over neurodegeneratie en hart- en vaatziekten.”
Waar hoop je over vijf jaar te staan?
“Tegen die tijd hoop ik dat we een succesvol klinisch onderzoek hebben afgerond en met ons CPP hebben bijgedragen aan een betere behandeling van kanker. Daarna duik ik misschien weer het lab in. Op naar het volgende CPP-medicijn waarmee we mensen kunnen behandelen. Tegen kanker of een andere ziekte, zoals Alzheimer or ALS. En natuurlijk tegen hart- en vaatziekten, zoals aneurysma's (zwakke plekken in slagaders – red.)”
“Dit is precies waarom ik het uitschakelen van senescente cellen zo interessant vind: het kan een oplossing bieden voor zoveel ziekten. We zien een levensverlenging van 27 procent bij muizen, waarbij de cognitieve en bewegingsfuncties tot het einde toe goed blijven. Dit zijn aanwijzingen dat het wegwerken van senescente cellen ook zou kunnen werken tegen bijvoorbeeld dementie. Ik vind het enorm uitdagend om dit verder te onderzoeken.”
Van promotie tot klinische trial
2004
Peter start zijn promotieonderzoek in UMC Utrecht. Hij bestudeert daar een specifieke groep eiwitten, de FOXO’s. Deze eiwitten spelen een belangrijke rol bij het tegengaan van verschillende soorten stress in cellen en daarmee met het in leven houden daarvan. Ze zijn betrokken bij onder meer de signalering van anti-oxidanten, groei, stofwisseling en levensduur van cellen. Na stress remmen ze de celdeling, en helpen ze bij het temperen van de stress in cellen. In deze periode kwam Peter erachter dat FOXO4 aan p53 kan binden: het begin van een lange reis naar het tegengaan van ziekten.
2009
Na zijn promotie vertrekt Peter naar San Francisco, VS. Daar ontdekt hij in 2009 dat het eiwit FOXO4 senescente cellen in leven houdt door het eiwit p53 te beteugelen. Op dat moment is er nog geen onderscheid in subtypen van senescente cellen. Het is ook pas net duidelijk dat die cellen factoren uitscheiden die bijdragen aan veroudering, maar niemand had nog bedacht dat je ze ook kan opruimen. Peter ontwikkelt zijn eerste twee zogeheten ‘CPP’s’ (celpenetrerende peptiden) om de verbinding tussen FOXO4 en p53 te verbreken. Een dergelijke CPP kan door celmembranen heen gaan en de senescente cellen met p53 doden.
2012
In 2012 keert Peter terug naar Nederland en vervolgt zijn onderzoek in Rotterdam, bij het Erasmus MC. Hier publiceert hij zijn bevindingen dat een derde generatie CPP’s, de FOXO4-DRI (van D-Retro-Inverso), de gezondheid van snel verouderende muizen een beetje kan verbeteren.
2018
Peter gaat terug naar waar zijn senescente ontdekkingsreis ooit begon: het UMC Utrecht. Hier leidt hij zijn eigen onderzoeksgroep en ook een biotech bedrijf, Cleara Biotech, om de ontwikkeling van een vierde generatie CPP’s professioneel aan te pakken. Door de jaren heen blijft Peter zijn CPP’s testen en verbeteren.
2026 en verder
Inmiddels zijn er vele versies in de vierde generatie getest, en de beste daarvan ook in muizenproeven tegen ouderdomsziekten en kanker. De ambitie is om in 2027 de eerste klinische onderzoeken met Peters CPP’s te starten, gericht op patiënten met p53-mutant borst- en darmkanker. De coördinatie van het klinische onderzoek wordt verzorgd door Peters biotechbedrijf Cleara Biotech, dat nauw verbonden is aan het UMC Utrecht.
Don’t try this at home
Peters lange en intensieve onderzoek is niet aan de buitenwereld voorbij gegaan. Helaas heeft dat ertoe geleid dat bedrijven ermee aan de haal zijn gegaan en preparaten op de markt brengen die veroudering en bepaalde ziekten zouden tegengaan. Peter en zijn team hebben niets met deze middelen te maken en raden het gebruik ervan ook af.
“Hoewel wij natuurlijk erg enthousiast zijn over de vorderingen met onze CPP’s, is het nog niet zo dat ze al geschikt zijn voor gebruik bij mensen. De CPP’s doden in principe met name slechte cellen. Echter, net als met alle medicijnen, kun je ook te hoog of te lang doseren. En dan gaan er ook gezonde cellen aan dood”, vertelt Peter.
“We zijn dit allemaal nog nauwkeurig aan het bepalen, en onderzoeken dit op een verantwoorde manier in klinische studies. Het is belangrijk dat behandelingen met dergelijke CPP’s onder begeleiding van een arts plaatsvinden. Hopelijk kunnen we dan ook écht mensen helpen.”
Meer informatie
- Peptiden Q&A: peptiden uitgelegd in 10 vragen en antwoorden.
- Associate professor-lezing Peter de Keizer: video waarin Peter de Keizer uitlegt wat senescente cellen zijn en hoe ze een rol spelen bij kanker en verouderingsziekten.


